Nhôm (Al) là một kim loại phổ biến, được ứng dụng rộng rãi trong cuộc sống hàng ngày. Các Tính Chất Hóa Học Của Nhôm đóng vai trò quan trọng trong việc quyết định ứng dụng của nó. Bài viết này sẽ đi sâu vào tìm hiểu các tính chất hóa học đặc trưng của nhôm, giúp bạn hiểu rõ hơn về kim loại thú vị này.
Tính Khử Mạnh Của Nhôm
Nhôm là kim loại có tính khử mạnh, dễ dàng nhường 3 electron lớp ngoài cùng để đạt cấu hình electron bền vững. Điều này thể hiện qua việc nhôm phản ứng với nhiều chất oxi hóa khác nhau.
Phản Ứng Với Oxi
Nhôm phản ứng mãnh liệt với oxi, tạo thành lớp oxit nhôm (Al2O3) mỏng, bền vững trên bề mặt. Lớp oxit này bảo vệ nhôm khỏi bị ăn mòn tiếp tục. Phản ứng này giải phóng nhiệt mạnh.
2Al + 3O2 → 2Al2O3
Phản Ứng Với Phi Kim Khác
Ngoài oxi, nhôm còn phản ứng với nhiều phi kim khác như clo, lưu huỳnh,… tạo thành các muối tương ứng. cách học hóa tốt sẽ giúp bạn hiểu rõ hơn về các phản ứng này.
2Al + 3Cl2 → 2AlCl3
2Al + 3S → Al2S3
Nhôm Tác Dụng Với Axit
Nhôm phản ứng với hầu hết các axit mạnh như HCl, H2SO4 loãng, tạo thành muối nhôm và giải phóng khí hydro. Tuy nhiên, nhôm không phản ứng với HNO3 và H2SO4 đặc nguội do bị thụ động hóa.
2Al + 6HCl → 2AlCl3 + 3H2
 Phản ứng của nhôm với axit
Phản ứng của nhôm với axit
Nhôm Tác Dụng Với Bazơ
Một tính chất đặc biệt của nhôm là khả năng phản ứng với cả axit và bazơ. Nhôm phản ứng với dung dịch bazơ mạnh như NaOH, KOH, tạo thành muối aluminat và giải phóng khí hydro.
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2
Nhôm Tác Dụng Với Nước
Mặc dù nhôm có lớp oxit bảo vệ, nhưng khi lớp oxit này bị phá hủy (ví dụ như trong môi trường kiềm), nhôm có thể phản ứng chậm với nước tạo thành Al(OH)3 và giải phóng khí hydro.
2Al + 6H2O → 2Al(OH)3 + 3H2
Nhôm Tác Dụng Với Dung Dịch Muối
Nhôm có thể đẩy các kim loại đứng sau nó trong dãy điện hóa ra khỏi dung dịch muối của chúng. Ví dụ, nhôm phản ứng với dung dịch CuSO4, tạo thành Al2(SO4)3 và kim loại Cu. hai học sinh trường quo tế tp hcm đã thực hiện thí nghiệm này trong giờ thực hành hóa học.
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
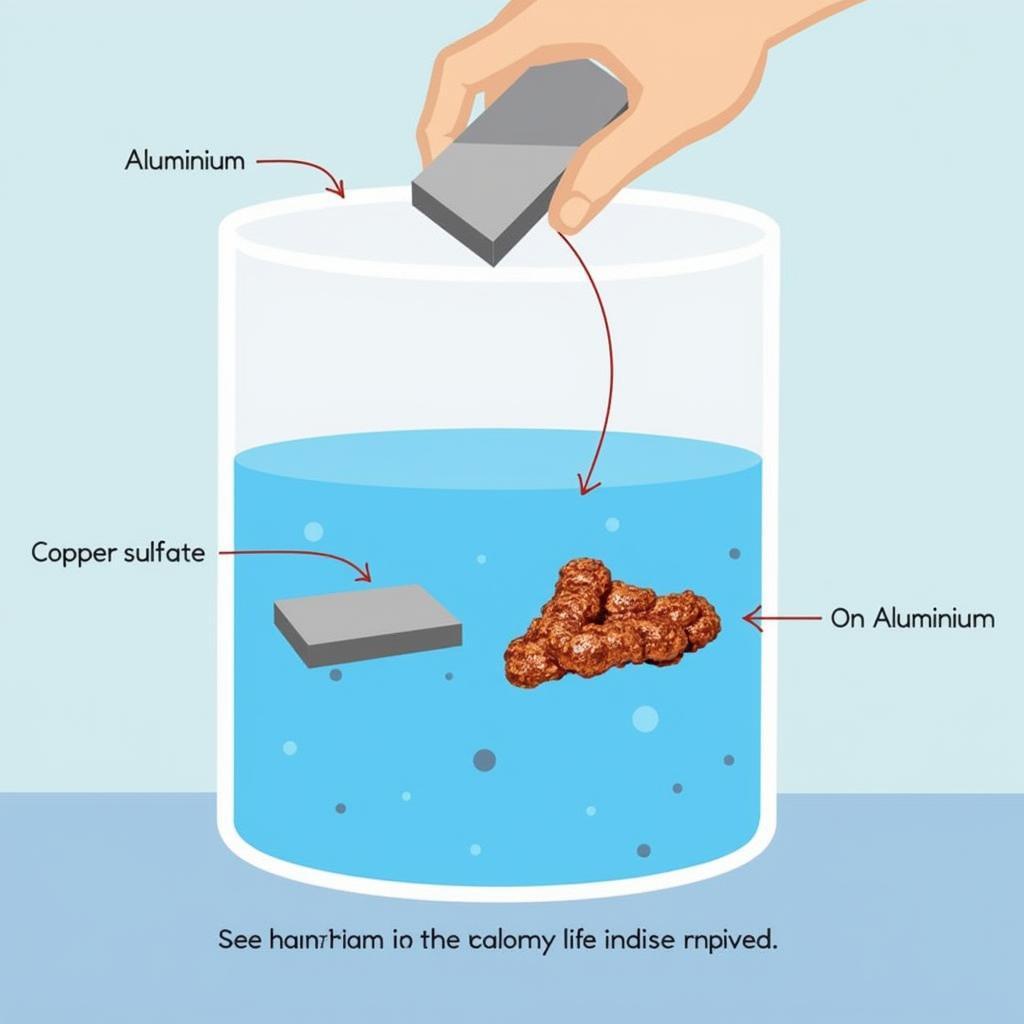 Phản ứng của nhôm với muối
Phản ứng của nhôm với muối
Kết luận
Các tính chất hóa học của nhôm, đặc biệt là tính khử mạnh, phản ứng với cả axit và bazơ, đã làm cho nhôm trở thành một kim loại quan trọng trong nhiều ứng dụng. Hiểu rõ các tính chất này là bước đầu tiên để khám phá tiềm năng ứng dụng rộng rãi của nhôm. công nghệ thông tin học những môn nào cũng liên quan đến việc ứng dụng nhôm trong lĩnh vực công nghệ.
FAQ
- Tại sao nhôm không phản ứng với HNO3 đặc nguội?
- Lớp oxit nhôm có vai trò gì?
- Ứng dụng của phản ứng nhôm với bazơ là gì?
- Tại sao nhôm được sử dụng rộng rãi trong đời sống?
- Làm thế nào để bảo quản các vật dụng bằng nhôm?
- Nhôm có độc hại không?
- chương trình tiếng anh tiểu học cambridge có liên quan đến tính chất hóa học của nhôm không?
Bạn có thể tìm hiểu thêm về cách xếp đồ vào vali đi du học trên website của chúng tôi.
Khi cần hỗ trợ hãy liên hệ Số Điện Thoại: 0705065516, Email: thptquangtrung@gmail.com Hoặc đến địa chỉ: NB tổ 5/110 KV bình thường b, P, Bình Thủy, Cần Thơ, Việt Nam. Chúng tôi có đội ngũ chăm sóc khách hàng 24/7.

